für Plastische Chirurgie
und Handchirurgie
Ein zentraler Forschungsschwerpunkt der Klinik ist die Entwicklung personalisierter regenerativer Therapien und ihre Überführung in die klinische Anwendung. Das Ziel: körpereigene Regenerationsmechanismen gezielt und sicher zu aktivieren, um geschädigte Zellen, Gewebe oder Organe mit den Ressourcen des Körpers selbst zu reparieren oder zu ersetzen.
Anders als bei konventionellen Verfahren der regenerativen Medizin – bei denen körperfremde oder modifizierte Stammzellen transplantiert werden, etwa aus Tierquellen, Embryonen, Nabelschnurblut, Knochenmark oder Fettgewebe – setzt dieser Ansatz auf eine zellfreie Strategie. Dabei werden körpereigene Signalmoleküle des Patienten genutzt, um die mesenchymalen Stammzellnischen im Zielorgan gezielt zu aktivieren.
Eine an der Klinik entwickelte spezielle Technologie ("Regenerative Signaling Technology") stimuliert dafür spezifische molekulare Signalwege, die für Gewebereparatur und funktionelle Wiederherstellung entscheidend sind. Gegenüber herkömmlichen Transplantationsverfahren reduziert dieser Ansatz typische Risiken wie Infektionen, Abstoßungsreaktionen oder unkontrolliertes Zellwachstum – und ermöglicht durch den Einsatz körpereigener Signale eine präzisere und potenziell wirksamere Behandlung.
Vorteile von personalisierten regenerativen Therapieverfahren
Abb.: Therapeutische Anwendungsmöglichkeiten personalisierter regenerativer Therapien:

Die Regenerative Signaling Technology ist ein medizinisches Verfahren, das die natürlichen Selbstheilungskräfte des Körpers gezielt aktiviert. Ziel ist es, geschädigte Zellen, Gewebe oder Organe nicht von außen zu ersetzen, sondern die körpereigenen Regenerationsmechanismen zu aktivieren – präzise, individuell und ohne den Einsatz körperfremder Substanzen.
Wissenschaftlicher Hintergrund:
Stammzellen tragen auf ihrer Oberfläche spezifische Rezeptoren, die auf bestimmte Signalmoleküle – sogenannte Zytokine und Chemokine – reagieren. Diese Botenstoffe koordinieren im gesunden Organismus Zellwachstum, Gewebereparatur und Entzündungsreaktionen. Bei Erkrankungen oder Gewebeschäden können diese Signalwege gestört oder erschöpft sein. Die Therapie setzt genau hier an: Sie stellt dem Körper das fehlende Signalprofil zur Verfügung, um die natürliche Regeneration wieder in Gang zu setzen.
1. Gewinnung des patientenspezifischen Signalprofils
Mithilfe eines patentierten Verfahrens (EP2809333) wird aus patienteneigenem Material ein individuelles Profil aus Zytokinen und Chemokinen gewonnen. Da die Botenstoffe körpereigen sind, ist die Verträglichkeit in der Regel sehr gut.
2. Systemische Applikation und gezielte Signalwirkung
Nach der Verabreichung gelangen die Signalmoleküle über den Blutkreislauf zu den betroffenen Gewebebereichen. Dort binden sie an spezifische Rezeptoren auf den Stammzellen und leiten die Regeneration gezielt ein.
3. Reaktivierung der Stammzellnischen
Die angesprochenen Stammzellnischen – also die spezialisierten Mikroumgebungen, in denen Stammzellen ruhen und aktiviert werden – nehmen ihre regulatorische Funktion wieder auf. Das Ergebnis: eine koordinierte, gewebeaufbauende Reaktion an genau den Stellen, wo sie benötigt wird.
Abb. 1 – Marker-Analyse
Bei der Regenerative Signaling Technology bleiben die charakteristischen Oberflächenmarker mesenchymaler Stammzellen (CD29, CD44, CD73, CD90, CD105, CD166) erhalten, während Marker anderer Zelllinien (z. B. CD34, CD31, CD71) nicht exprimiert werden. Das Zellprofil bleibt auch nach wiederholter Stimulation stabil und zeigt keine Hinweise auf unkontrolliertes Wachstum. (1)
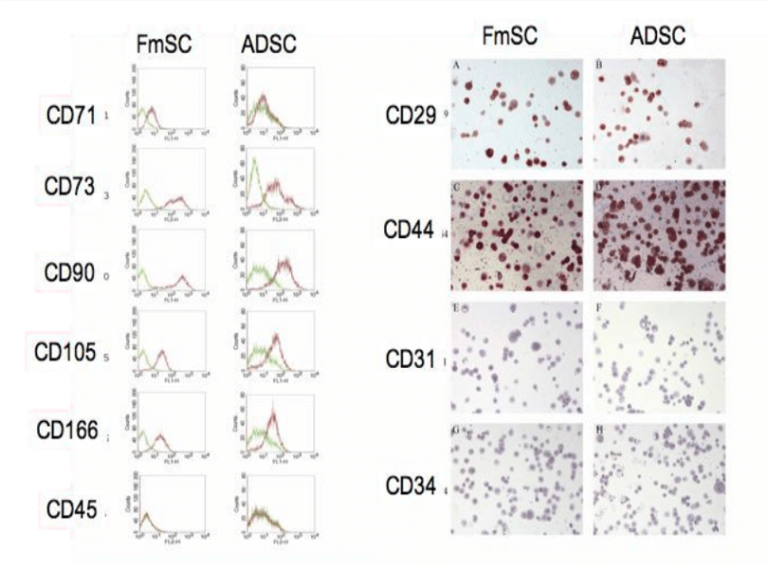
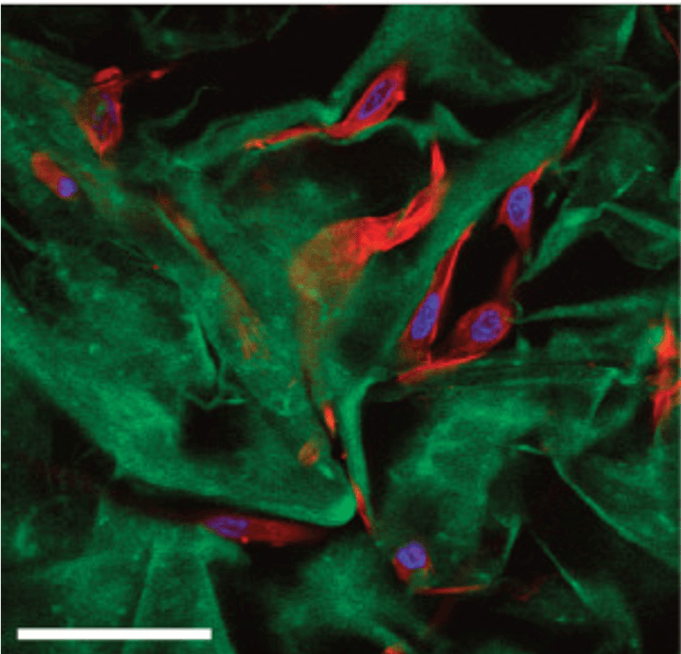
Abb. 2 – Fluoreszenzmikroskopische Darstellung nach Stimulation
Bei der Regenerative Signaling Technology reagieren Stammzellen auf gezielte körpereigene Signale. Die Aufnahme zeigt die Zellen nach dieser Stimulation: Die Zellkerne sind blau dargestellt, das Zellgerüst grün und weitere Zellbestandteile rot.
Die Zellen bleiben strukturell intakt und passen ihre Aktivität an die erhaltenen Signale an. Je nach Bedarf können sie sich vermehren oder sich zu spezialisierten Zellen weiterentwickeln. (2)
(1)Bader A, ….Machens HG: Rejuvenation Research 14,1: 57-66 (2011)
(2)Danner S, ….Machens HG, Egana T: J Invest Dermatol 132 (6): 1707-16 (2012)